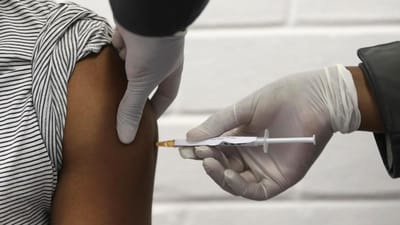
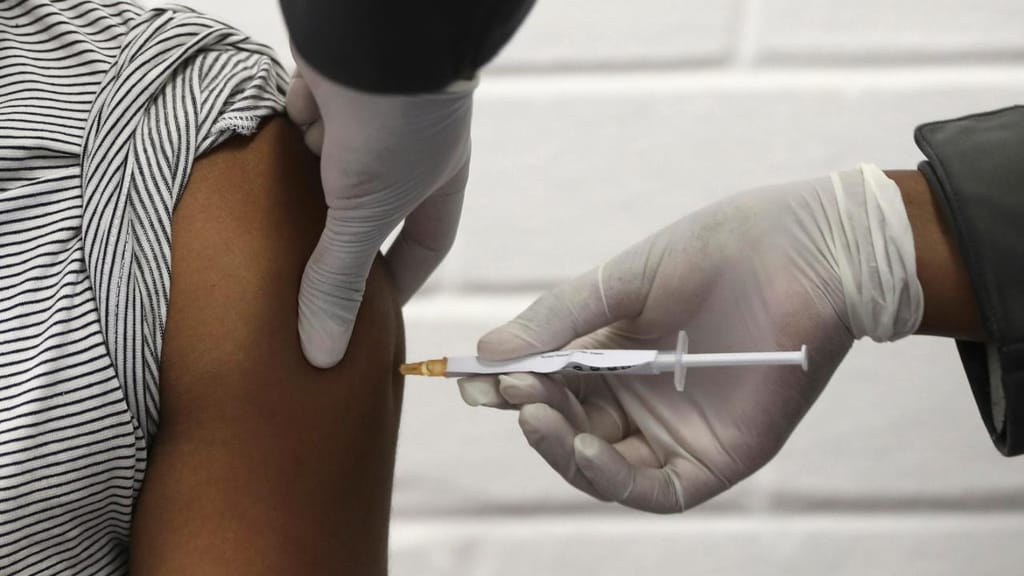
A Agência Nacional de Vigilância Sanitária (Anvisa) do Brasil aprovou esta quinta-feira, por unanimidade, a criação de um sistema que prevê a concessão de uma autorização temporária para o uso de emergência de vacinas contra a covid-19.
A utilização, que terá caráter experimental, deve fazer acelerar os processos de aprovação das vacinas desenvolvidas pela AstraZeneca, Pfizer, Johnson & Johnson's, Coronavac e Sinovac.
A agência já tinha definido que o uso de emergência devia obedecer a certos critérios, nomeadamente os resultados apresentados nas fases 3 de cada ensaio, onde ainda não chegaram as experiências da Johnson & Johnson's e da Coronavac. Acresce ainda que esses ensaios clínicos devem ser desenvolvidos no Brasil.
A autorização de uso de emergência é um mecanismo que pode facilitar a disponibilização e o uso de vacinas contra a covid-19, ainda que não tenham sido avaliadas pelos registos, desde que cumpram os requisitos mínimos de segurança, qualidade e eficácia", afirmou a diretora da Anvisa, Alessandra Bastos Soares, em declarações reproduzidas pelo portal G1.
As vacinas aprovadas neste sistema temporário vão ser utilizadas em programas públicos de vacinação que serão coordenados pelo Ministério da Saúde.
A Anvisa informou ainda que não foi feita, até ao momento, qualquer solicitação para a utilização de emergência ou registo das vacinas que estão em desenvolvimento no Brasil.
A agência ressalva que poderá modificar, suspender ou cancelar a autorização temporária a qualquer momento.
O Brasil ultrapassou esta quarta-feira a barreira das 6,7 milhões de infeções pelo novo coronavírus (6.728.452), após ter contabilizado 53.453 novos casos, informou o Ministério da Saúde.
Em relação ao número de mortes, o país sul-americano somou 836 óbitos, totalizando 178.995 vítimas mortais devido à covid-19.